日前,專注于生命科學(xué)領(lǐng)域的全球性公司IQVIA發(fā)布了分析細(xì)胞和基因療法現(xiàn)狀和未來(lái)發(fā)展趨勢(shì)的研究報(bào)告。報(bào)告表示,細(xì)胞和基因療法能給沒(méi)有其它治療選擇的患者帶來(lái)變革性獲益,近年來(lái)這一領(lǐng)域的投資、臨床研究和新產(chǎn)品上市均達(dá)到新高。該報(bào)告同時(shí)指出影響這一領(lǐng)域未來(lái)發(fā)展的8大因素。今天這篇文章里,藥明康德內(nèi)容團(tuán)隊(duì)將與讀者介紹這篇報(bào)告的精彩內(nèi)容。
對(duì)細(xì)胞和基因療法的信心和興趣不斷提升,新興公司為創(chuàng)新源泉
細(xì)胞和基因療法的早期進(jìn)展和在臨床上取得的不斷成功,讓在這一領(lǐng)域的大藥企和新興醫(yī)藥公司都有機(jī)會(huì)獲得大量投資,支持在細(xì)胞和基因療法領(lǐng)域的持續(xù)創(chuàng)新。IQVIA的報(bào)告指出,與10年前相比,細(xì)胞和基因療法領(lǐng)域的交易增加了48%,在所有生命科學(xué)交易中的占比也不斷提高,在2023年超過(guò)10%,2014年這一數(shù)值只有5%。這些數(shù)據(jù)顯示了業(yè)界對(duì)細(xì)胞和基因療法治療模式的信心和興趣。
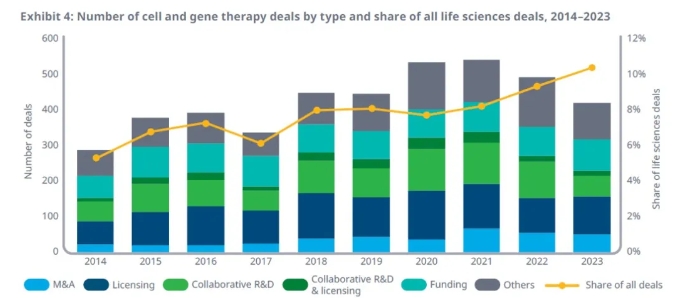
▲細(xì)胞和基因療法領(lǐng)域交易數(shù)目和占所有生命科學(xué)交易的比例在過(guò)去10年里顯著提升(圖片來(lái)源:IQVIA官網(wǎng))
幾乎所有的交易都與新興生物醫(yī)藥公司(EBP,定義為年銷售額小于5億美元,每年研發(fā)投入小于2億美元的公司)有關(guān),從2018年到2023年,涉及兩家或多家公司的交易中,新興生物醫(yī)藥公司之間的交易占三分之二,大型公司與新興生物公司之間的交易占接近三分之一,而大藥企之間的交易非常少。這些數(shù)據(jù)顯示,在細(xì)胞和基因療法領(lǐng)域,新興生物醫(yī)藥公司是創(chuàng)新和新技術(shù)平臺(tái)的主要源泉。
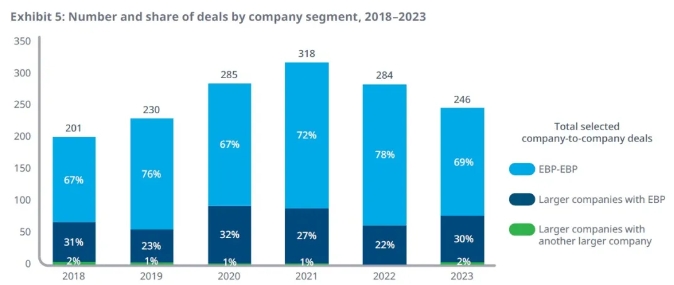
▲細(xì)胞和基因療法領(lǐng)域交易按照公司大小的分類(圖片來(lái)源:IQVIA官網(wǎng))
產(chǎn)業(yè)界臨床開發(fā)活動(dòng)達(dá)到新高
報(bào)告指出,過(guò)去5年中總計(jì)3285項(xiàng)臨床試驗(yàn)啟動(dòng),評(píng)估細(xì)胞和基因療法在不同類型患者中的作用。在2023年,631項(xiàng)臨床試驗(yàn)啟動(dòng)。其中生物醫(yī)藥公司啟動(dòng)的臨床試驗(yàn)占比64%。產(chǎn)業(yè)界啟動(dòng)的臨床試驗(yàn)的數(shù)量在過(guò)去10年中大幅度提升,與2013年相比提高了276%,與5年前相比提高了34%,并在2023年達(dá)到新高。
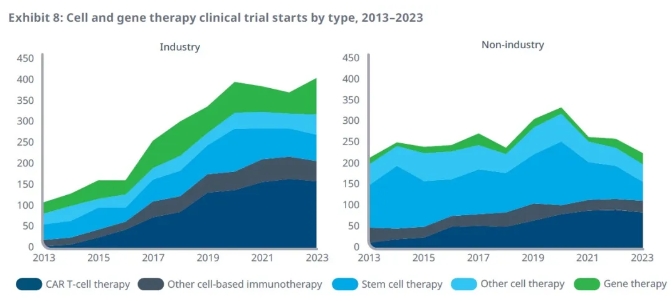
▲生物醫(yī)藥公司啟動(dòng)的細(xì)胞和基因療法臨床試驗(yàn)在過(guò)去10年里大幅度增加(圖片來(lái)源:IQVIA官網(wǎng))
這些臨床試驗(yàn)的增加主要來(lái)自CAR-T細(xì)胞療法的臨床試驗(yàn),值得一提的是,在2023年,生物醫(yī)藥公司啟動(dòng)的CAR-T療法臨床試驗(yàn)的占比與2022年相比有所下降,而基因療法的占比從2022年的14%提高到22%,顯示了行業(yè)聚焦領(lǐng)域轉(zhuǎn)移的跡象。
在治療領(lǐng)域方面,CAR-T療法的主要治療領(lǐng)域仍然為血液癌癥和實(shí)體瘤,不過(guò)雖然靶向自身免疫性疾病的臨床試驗(yàn)不多,但近期的研究結(jié)果顯示了CAR-T療法在這一領(lǐng)域的潛力。近日在《新英格蘭醫(yī)學(xué)雜志》上發(fā)表的一項(xiàng)研究中,CAR-T細(xì)胞療法讓100%的患者獲得緩解并持續(xù)停止使用免疫抑制藥物。
基因療法治療的疾病領(lǐng)域更為多樣化,其中治療實(shí)體瘤的臨床試驗(yàn)占比35%,此外,神經(jīng)疾病、代謝、內(nèi)分泌、心血管和眼科疾病領(lǐng)域均有顯著臨床開發(fā)活動(dòng)。基因療法往往用于治療遺傳病,并給可能面對(duì)終身殘疾威脅的患者帶來(lái)希望。比如,今年初,禮來(lái)公司和復(fù)旦大學(xué)的研究團(tuán)隊(duì)分別報(bào)告了各自的基因療法治療遺傳性耳聾兒童的臨床試驗(yàn)結(jié)果。在兩項(xiàng)臨床試驗(yàn)中,接受基因療法治療的兒童的聽力都獲得顯著改善。
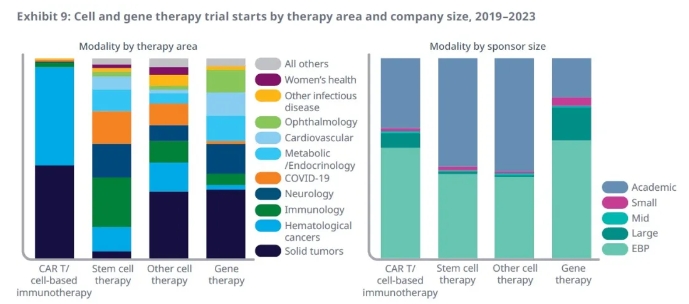
▲臨床期細(xì)胞和基因療法治療的疾病領(lǐng)域以及啟動(dòng)這些臨床試驗(yàn)的機(jī)構(gòu)分類(圖片來(lái)源:IQVIA官網(wǎng))
已有細(xì)胞和基因療法臨床試驗(yàn)中,超過(guò)90%由新興生物醫(yī)藥公司和學(xué)術(shù)研究所啟動(dòng)。其中新興生物醫(yī)藥公司支持50%的臨床試驗(yàn),主要聚焦于CAR-T細(xì)胞療法和基因療法。而學(xué)術(shù)研究所支持41%的臨床試驗(yàn)活動(dòng),代表著大部分干細(xì)胞和CAR-T療法之外的其它細(xì)胞療法研究。
大型醫(yī)藥公司啟動(dòng)的臨床試驗(yàn)占比6%,幾乎全部聚焦于基于細(xì)胞的免疫療法和基因療法。它們更可能在收購(gòu)新興醫(yī)藥公司或與其達(dá)成研發(fā)合作后,將已經(jīng)獲得前期臨床試驗(yàn)積極結(jié)果的項(xiàng)目推入后期臨床開發(fā)。
獲批療法數(shù)目翻倍,全球監(jiān)管機(jī)構(gòu)助力加速產(chǎn)品上市
報(bào)告指出,截至2023年底,總計(jì)76款細(xì)胞和基因療法獲得全球監(jiān)管機(jī)構(gòu)的批準(zhǔn)上市,與2013年的總數(shù)相比翻了一倍以上。在過(guò)去3年中,20款細(xì)胞和基因療法獲批上市。
在這些獲批療法中,CAR-T療法和其它基于細(xì)胞的癌癥免疫療法在過(guò)去10年中進(jìn)展迅速,截至2023年底已有12款療法獲批。19款基因療法在全球范圍內(nèi)獲批,主要用于治療遺傳病。
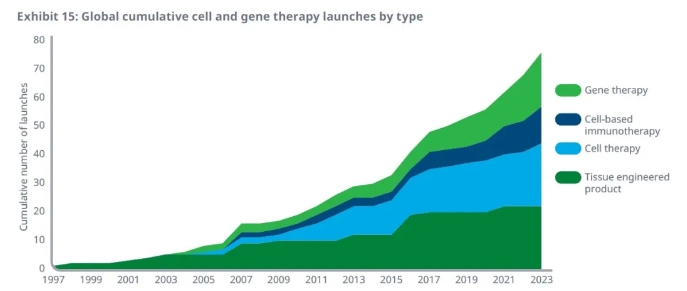
▲全球獲批細(xì)胞和基因療法數(shù)目和療法類型(圖片來(lái)源:圖片來(lái)源:IQVIA官網(wǎng))
在2023年,多款獲批的細(xì)胞和基因療法代表著針對(duì)疾病領(lǐng)域的重大突破。比如,首款治療1型糖尿病的細(xì)胞療法獲得批準(zhǔn)。首款治療杜氏肌營(yíng)養(yǎng)不良的基因療法獲得批準(zhǔn)。在2023年,首個(gè)可重復(fù)給藥的基因療法也獲得美國(guó)FDA的批準(zhǔn)上市。
在監(jiān)管審評(píng)方面,隨著細(xì)胞和基因療法研發(fā)活動(dòng)的不斷擴(kuò)展,全球的監(jiān)管機(jī)構(gòu)也不斷推出新的舉措來(lái)加速研發(fā)項(xiàng)目的開發(fā)和審評(píng)。以美國(guó)為例,IQVIA報(bào)告指出,過(guò)去5年批準(zhǔn)的細(xì)胞和基因療法中,高達(dá)86%使用了至少一種FDA加速研發(fā)的資格認(rèn)定。其中,71%的療法獲得突破性療法認(rèn)定,64%的療法獲得快速通道資格,均遠(yuǎn)遠(yuǎn)高于非細(xì)胞和基因療法。這些數(shù)字顯示細(xì)胞和基因療法通常被用于治療嚴(yán)重、并具有顯著未竟需求的疾病。
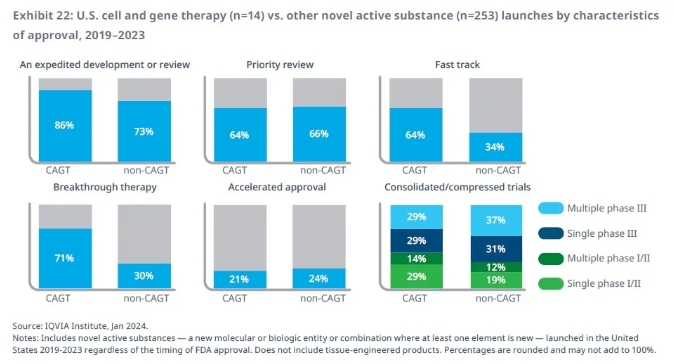
▲2019-2023年獲批上市的細(xì)胞和基因療法(CAGT)與非細(xì)胞和基因療法(non-CAGT)的特征(圖片來(lái)源:IQVIA官網(wǎng))
此外,F(xiàn)DA還推出再生醫(yī)藥先進(jìn)療法(RMAT)認(rèn)定,這一認(rèn)定為合格的項(xiàng)目同時(shí)提供快速通道資格和突破性療法認(rèn)定的幫助。
在全球范圍內(nèi),其它監(jiān)管機(jī)構(gòu)也為細(xì)胞和基因療法的開發(fā)提供了加速渠道,比如歐洲藥品管理局(EMA)的PRIME認(rèn)定,加速評(píng)估和有條件上市,澳大利亞監(jiān)管機(jī)構(gòu)的優(yōu)先審評(píng)和有條件批準(zhǔn),日本監(jiān)管機(jī)構(gòu)的SAKIGAKE認(rèn)定。
細(xì)胞和基因療法的未來(lái)
報(bào)告指出,細(xì)胞和基因療法在過(guò)去10年里已經(jīng)獲得了長(zhǎng)足的進(jìn)步,不過(guò)這一產(chǎn)業(yè)與小分子藥物和抗體領(lǐng)域相比,仍然處于未成熟階段,未來(lái)的發(fā)展仍然存在很多不確定性。細(xì)胞和基因療法產(chǎn)業(yè)的未來(lái)發(fā)展依賴于產(chǎn)品研發(fā)活動(dòng)、監(jiān)管批準(zhǔn)、患者可及性、療法的長(zhǎng)期療效和安全性等8個(gè)指標(biāo)的進(jìn)展。
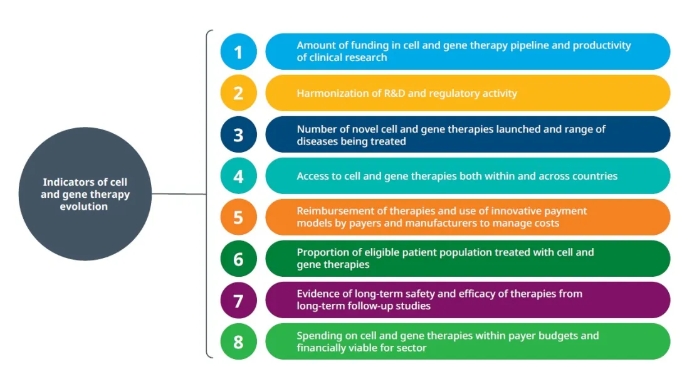
▲評(píng)估細(xì)胞和基因療法未來(lái)發(fā)展的8個(gè)指標(biāo)(圖片來(lái)源:IQVIA官網(wǎng))
2023年細(xì)胞和基因療法的獲批數(shù)目創(chuàng)下新的紀(jì)錄,報(bào)告預(yù)測(cè),隨著監(jiān)管審評(píng)的加速,以及細(xì)胞和基因療法在腫瘤學(xué)以外的潛力得到關(guān)注,未來(lái)全球每年可能批準(zhǔn)12款以上的細(xì)胞和基因療法,其中一半療法治療腫瘤學(xué)以外的疾病領(lǐng)域,有望造福患者人數(shù)超過(guò)1萬(wàn)的更大型疾病。期待學(xué)術(shù)機(jī)構(gòu)、產(chǎn)業(yè)界、監(jiān)管機(jī)構(gòu)等方面的共同努力讓這一未來(lái)早日到來(lái)。
參考資料:
[1] Strengthening Pathways for Cell and Gene Therapies: Current State and Future Scenarios. Retrieved March 31, 2024, from https://www.iqvia.com/insights/the-iqvia-institute/reports-and-publications/reports/strengthening-pathways-for-cell-and-gene-therapies